继2022年11月、2023年8月、2024年3月港交所递表后,9月26日,维昇药业第四次向港交所递交招股书。
成立于2018年的维昇药业是港股唯一专注内分泌领域且研发长效生长激素的biotech(生物科技公司),有望成为港股“生长发育第一股”。
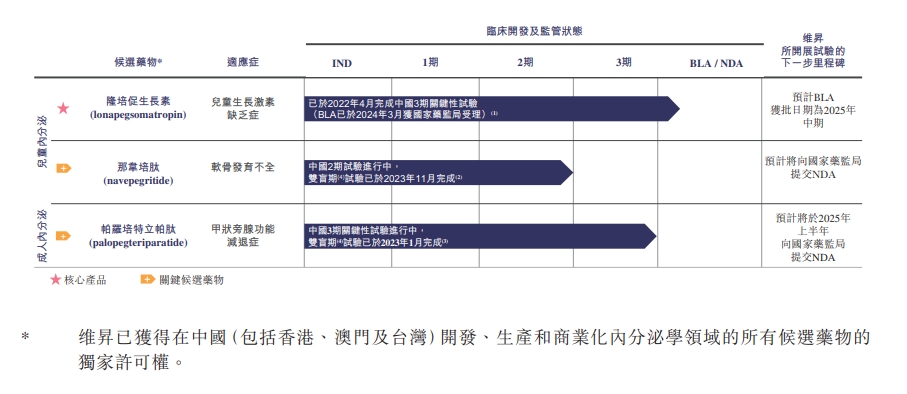
维昇药业产品管线
目前,维昇药业的产品管线包括三款候选药物,包括隆培促生长素、那韦培肽、帕罗培特立帕肽,分别用于治疗儿童生长激素缺乏症、软骨发育不全、甲状旁腺功能减退症。这三款药物是从维昇药业的合作伙伴及控股股东之一Ascendis Pharma授权引入。
2018年11月,维昇药业分别就三款产品与丹麦生物制药公司Ascendis Pharma订立三份独家许可协议,该协议于2021年1月进行了修订。通过协议,维昇药业获得在中国开发、生产和商业化三款候选药物。根据相关独家许可协议,维昇药业并没有支付任何特许权使用费或里程碑付款,而是向Ascendis Pharma A/S 的三家全资附属公司发行共计4000万股A轮优先股作为订立该等协议的对价。也就是说,Ascendis Pharma以产品入股,成为维昇药业的创始股东之一。
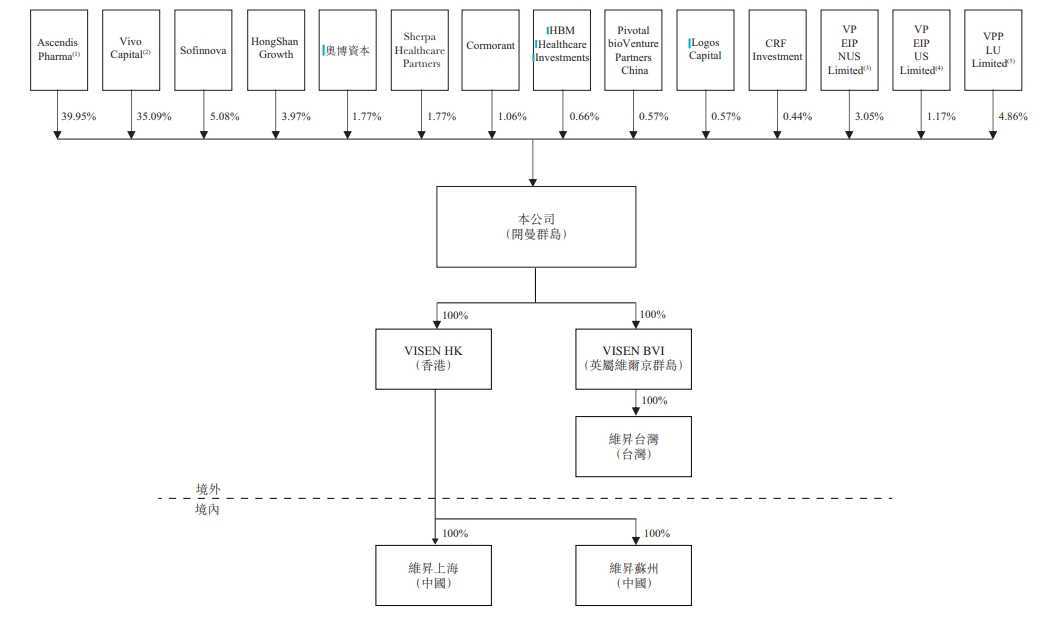
维昇药业股权结构 来源:招股书
招股书显示,Ascendis Pharma A/S、Ascendis附属公司及Vivo Funds是维昇药业的控股股东,于最后实际可行日期,Ascendis Pharma A/S通过其三家全资附属公司持有合计约39.95%股份,Vivo Plenilune IX Limited(或Vivo Capital)持有约35.09%的股份。
维昇药业在招股书的风险因素提到,公司开发、生产和商业化候选药物的权利受限于Ascendis Pharma授予的许可条款及条件。倘公司未能履行独家许可协 议中的义务,可能会失去开发、生产和商业化候选药物的权利,并须支付金钱损害赔偿,这可能对我们的业务营运造成重大不利影响。此外,2025年预期的商业化之后直至2028年,预计将向Ascendis Pharma采购核心产品以进行商业化供应,这可能会使公司面临潜在的供应链中断、 对产品供应的质量和时间缺乏控制等风险,并可能对我们的业务和盈利能 力造成不利影响。
三款产品中最接近商业化的是隆培促生长素,在全球已获美国FDA及欧盟EMA批准,其在中国3期关键试验已完成,BLA(生物制品许可申请)于2024年3月获国家药监局受理,预计获批时间为2025年中期。据Ascendis 2023年年报,该药在2023年销售额1.79亿欧元,预计2024年销售额将达2.2亿元至2.4亿欧元。
在生长激素赛道,国内有长春高新(000661.SZ)旗下金赛药业、安科生物(300009.SZ)、特宝生物(688278.SH)等A股上市公司布局。对于自家产品的优势,维昇药业称,隆培促生长素(lonapegsomatropin) 是唯一一款于每周给药之间在体内持续释放未经修饰的人生长激素的长效生长激素,与每日一次人生长激素相比,该产品提供了方便的给药方案,注射频率为每周一次,可能会提高儿童患者在日常生活中给药的依 从性。
另一款生长发育疾病领域产品是用于儿童软骨发育不全的治疗药物那韦培肽。软骨发育不全此前被纳入国家第二批罕见病目录,据维昇药业介绍,这是我国迄今为止唯一一款正在进行临床开发的可针对软骨发育不全病因治疗的药物。该产品已同时获得美国食品和药品监督管理局和欧盟委员会授予的孤儿药资格认定,目前在中国实现与全球同步开展二期临床实验。
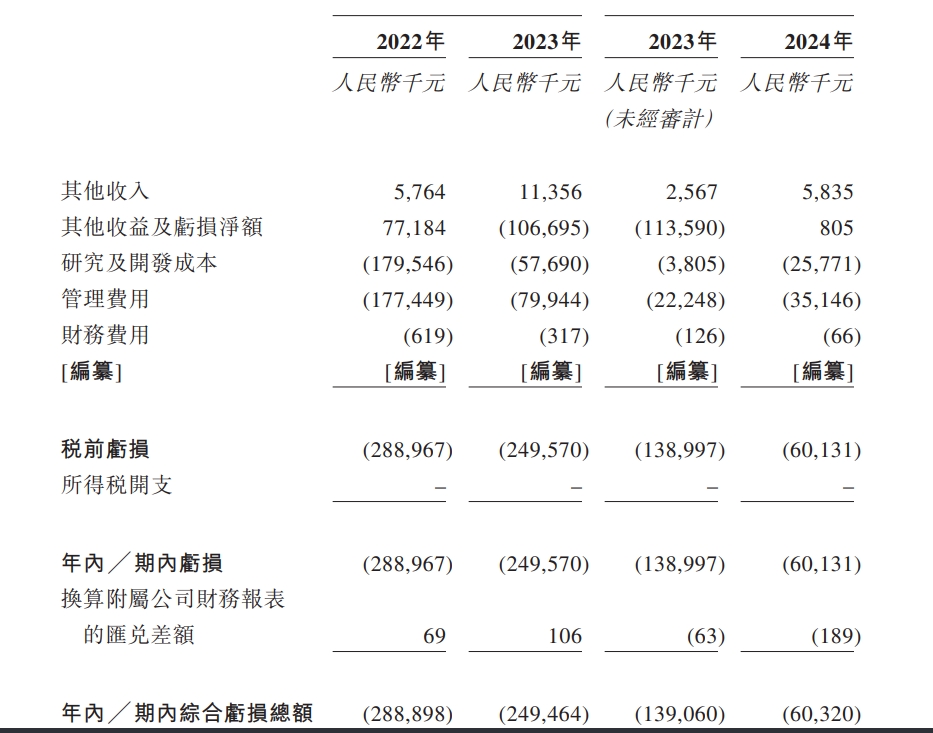
维昇药业财务数据
由于尚未有产品上市,维昇药业尚处于未盈利状态。招股书显示,2022年、2023年、2024年1-4月,期内综合亏损总额分别为2.89亿元、2.5亿元、6032万元。维昇药业提到,公司绝大部分经营亏损乃由研发开支、管理费用及其他收益及亏损净额所致,预计在未来几年将继续产生亏损。
维昇药业的首席执行官兼执行董事是卢安邦,负责公司的总体发展战略及业务方向。卢安邦曾在施维雅、武田等跨国药企工作,于2010年至2017年间担任日本药企武田药品工业株式会社的总经理、总裁及大中华区总裁,其任职期间,武田于中国的销售收入增长十倍以上。
陈军于2021年4月加入维昇药业担任首席商务官。招股书显示,陈军拥有超过20年的内分泌药物商业化经验,先后在诺和诺德、美敦力、礼来等知名跨国药企任职。
目前,维昇药业完成两轮融资,包括2018年11月,维昇药业完成A轮4000万美元融资,2021年1月完成1.5亿美元B轮融资。招股书显示,港股融资的用途也主要围绕三款核心产品,包括为正在进行的进口核心产品的BLA注册,正在进行的及计划中的本地生产核心产品的研发及BLA注册,计划中的新适应证扩展临床试验,以及核心产品隆培促生长素的计划商业化上市提供资金。







 京公网安备11000000000001号
京公网安备11000000000001号 京ICP备11000001号
京ICP备11000001号